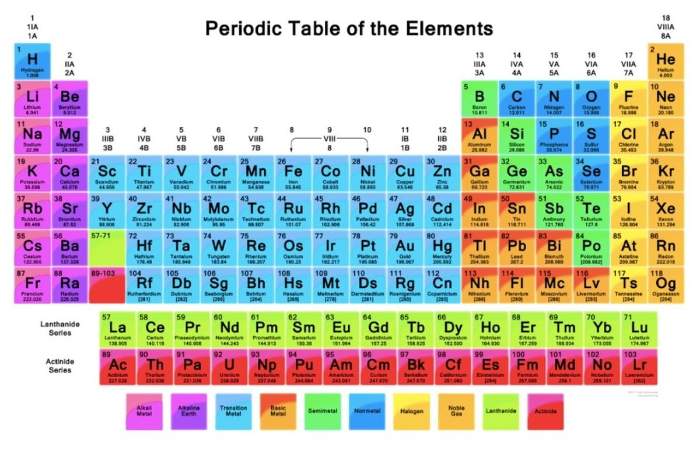
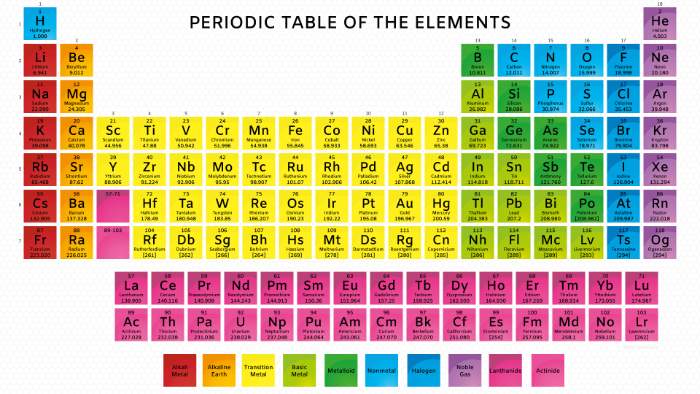
Luarbiasa.id-Tabel periodik sebenarnya sudah diajarkan di bangku SMA, khususnya saat pelajaran ilmu kimia. Secara sekilas, tabel ini mungkin tampak rumit dan membingungkan. Tapi sebenarnya tabel ini sangat membantu dalam mengidentifikasi berbagai unsur kimia dengan lebih mudah.
Memahami berbagai unsur kimia yang ada di dalam tabel tidak sesulit yang dibayangkan. Agar bisa lebih memahami isi tabel ini, pelajadi seluk-beluk tabel secara menyeluruh. Pertama, pahami dulu pengertiannya sebelum mempelajari yang lainnya.
Pengertian Tabel Periodik
Merupakan suatu tabel yang isinya berupa berbagai unsur kimia lengkap dengan nomor atom yang dimiliki oleh setiap unsur kimia. Setiap nomor atom berisi proton dalam jumlah tertentu dan konfigurasi elektron tertentu. Ada empat blok yang terdapat dalam tabel ini, yaitu blok f, d, p, dan s.
Dalam satu baris atau periode yang ada di sebelah kiri, terdapat sifat logam. Dan di bagian kanan menunjukkan unsur yang bersifat non logam. Dalam tabel kimia ini, ada beberapa istilah yang digunakan. Jika ingin memahami tabel ini, pastikan untuk mempelajari semua istilahnya.
1. Periode
Merupakan suatu bagian horizontal yang ada di dalam tabel kimia. Tren horizontal yang ada di bagian ini lebih siginifikan daripada tren vertikal karena sulit untuk dipahami. Misalnya, di blok f terdapat tanda aktinida dan lantanida yang membentuk dua unsur horizontal.
Keduanya bisa menjadi suatu definisi substansial untuk menentukan unsur kimia. Selain periode, masih ada beberapa istilah lainnya dalam tabel kimia.
2. Golongan
Dalam tabel yang berisi unsur utama dan berbagai unsur kimia, terdapat golongan yang juga dikenal dengan nama famili. Istilah ini menunjukkan bagian di dalam tabel yang membentuk kolom vertikal dengan tren periodik. Jadi bukannya menggunakan blok atau golongan periode tertentu.
3. Blok S
Dalam tabel kimia, blok S merupakan unsur yang terdiri dari dua golongan berbeda. Golongan pertama adalah logam alkali dan golongan kedua merupakan alkali tanah. Dalam susunannya, blok S juga mengandung berbagai unsur tambahan dengan helium dan hidrogen.
4. Blok P
Blok P mempunyai enam golongan, mulai dari golongan 13 hingga golongan 18. Nomor pada golongan ini diberikan sesuai dengan ketentuan IUPAC yaitu dimulai dari nomor 3A sampai nomor 8A, mengikuti sistem penamaan Amerika. Seluruh bagian blok P mempunyai metaloid sebagai kandungan utama.
5. Blok D
Dalam tabel periodik kimia, blok D mempunyai beberapa golongan, mulai dari golongan 3 hingga golongan 12. Dalam sistem penggolongan Amerika, yang termasuk dalam blok D adalah golongan 3B sampai golongan 2B. Seluruh unsur yang ada dalam blok D merupakan logam transisi.
6. Blok F
Seringkali, blok F dalam tabel kimia diletakkan pada bagian bawah. Golongan yang ada dalam blok ini tidak mempunyai nomor golongan. Beberapa unsur kimia yang termasuk dalam blok ini antara lain oganesson, tennessine, moscovium, nihonium, dan sebagainya.
Klasifikasi Tabel Unsur-Unsur Kimia
Pengelompokan berbagai unsur kimia dilakukan berdasarkan sifat kimia dan fisika sesuai dengan gejala yang dialami oleh setiap unsur tersebut. Memahami klasifikasi unsur kimia sangat penting agar bisa lebih memahami cara membaca tabel kimia dengan benar. Berikut ini klasifikasi unsur kimia.
1. Sifat-sifat umum
Setiap unsur kimia mempunyai sifat kimia dan fisika dengan tiga kategori berbeda, yaitu nonlogam, metalloid, dan logam. Agar lebih mengerti sifat umum di setiap unsur kimia, pahami keterangannya di bawah ini.
Logam
Berupa padatan berkilau yang mempunyai konduktivitas tinggi serta bisa membentuk alloy dengan berbagai bentuk logam yang lain. Sehingga senyawa iron yang berupa garam bisa terbentuk dengan nonlogam. Karakteristik logam di dalam tabel adalah:
| Berada di bagian sebelah kiri tabel unsur-unsur kimia. |
| 78% dari seluruh unsur yang bisa dikenali berupa logam. |
| Biasanya akan memadat di suhu ruangan. |
| Merupakan penghantar listrik dan panas yang baik. |
| Titik didih dan titik leleh unsur logam lebih tinggi. |
| Bisa ditempa serta direnggangkan. |
Nonlogam
Berbentuk gas tidak berwarna atau berwarna dan bisa membentuk senyawa secara kovalen dengan nonlogam yang lain. Seperti halnya logam, nonlogam juga mempunyai karakteristik tertentu di dalam tabel periodik, yaitu:
| Berada di sebelah kanan atas tabel unsur-unsur kimia. |
| Tidak bisa menghantarkan listrik dan panas dengan baik. |
| Titik didih dan titik leleh rendah. |
| Biasanya berbentuk gas atau padatan di suhu kamar. |
| Terdapat 22 unsur non-logam. |
Metaloid
Bersifat nonlogam dan logam atau bisa juga berupa campuran dari dua unsur tersebut.
2. Keadaan materi
Hal lain yang mempengaruhi pengelompokan unsur dalam tabel kimia adalah fase unsur atau wujud materi, seperti gas, padat, atau cair dalam tekanan dan temperatur standar. Unsur dengan wujud padat biasanya akan mempunyai tekanan atmosfer dan temperatur konvensional.
Unsur yang wujudnya cair hanya raksa dan brom dengan temperatur 0 derajat Celcius atau kurang lebih 32 derajat Fahrenheit pada tekanan atmosfer normal.
3. Titik didih dan titik lebur
Merupakan dua hal yang digunakan dalam mendefinisikan setiap karakter unsur. Dua hal ini dinyatakan dengan menggunakan satuan derajat Celcius di tekanan atmosfer tertentu. Klasifikasi unsur menggunakan dua titik ini sebenarnya sudah diketahui.
Tapi ada unsur radioaktif yang jumlahnya sangat kecil sehingga titik didih dan titik leburnya belum diketahui. He atau helium hanya mempunyai titik didih tanpa mempunyai titik lebur di dalam penyajian tabel periodic. Unsur ini tetap ada di wujud cair meskipun tekanan atmosfer ada dalam kondisi nol.
4. Massa jenis
Pengelompokan unsur dalam tabel kimia juga seringkali memanfaatkan massa jenis yang ada pada tekanan dan temperatur standar. Massa jenis dinyatakan dengan satuan g/cm3 atau gram per centimeter kubik. Massa jenis ini juga bisa dinyatakan untuk beberapa unsur gas.
Misalnya, ketika suatu unsur gas dipadatkan atau dicairkan, unsur tersebut akan mempunyai massa jenis yang kurang lebih sama dengan beberapa unsur kimia yang lain.
5. Struktur kristal
Unsur kimia yang diteliti hingga saat ini mempunyai delapan jenis struktur kristal. Kedelapan struktur kristal tersebut adalah tetragonal, rhombohedral, ortorombik, monokinis, heksagonal, kubus pusat muka, kubik pusat badan, dan kubik.
Dalam beberapa unsur transuranium sintetis, tersedia sampel yang jumlahnya sangat sedikit sehingga struktur kristalnya tidak bisa ditentukan dengan mudah.
6. Asal usul di permukaan bumi
Terdapat 94 unsur kimia yang pembentukannya terjadi secara alami dan ada 24 unsur lainnya yang proses pembentukannya terjadi secara artifisial. Ke-24 unsur tersebut terbentuk sebagai suatu produk sintesis yang dibuat melalui reaksi nuklir buatan.
Saat ini, 83 unsur kimia mempunyai radioaktif lemah dan mempunyai sifat stabil serta dianggap sebagai primordian. Sedangkan 11 unsur lainnya mempunyai waktu paruh cukup singkat pada awal semesta sehingga dianggap sebagai unsur fanal.
Unsur Kimia dalam Tabel Periodik Lengkap
Berdasarkan informasi di atas, secara keseluruhan ada 118 unsur dalam tabel unsur-unsur kimia. Masing-masing mempunyai nomor atomnya sendiri serta simbol yang mewakilinya. Biasanya, simbol unsur kimia lebih sering digunakan daripada nama unsur kimia itu sendiri.
Pelajari daftar lengkap unsur kimia dalam tabel berikut ini.
| No. Atom | Simbol | Unsur Kimia | No. Atom | Simbol | Unsur Kimia |
| 1 | H | Hidrogen | 60 | Nd | Neodymium |
| 2 | He | Helium | 61 | Pm | Promethium |
| 3 | Li | Lithium | 62 | Sm | Samarium |
| 4 | Be | Beryllium | 63 | Eu | Europium |
| 5 | B | Boron | 64 | Gd | Gadolinium |
| 6 | C | Carbon | 65 | Tb | Terbium |
| 7 | N | Nitrogen | 66 | Dy | Dysprosium |
| 8 | O | Oxygen | 67 | Ho | Holmium |
| 9 | F | Fluorine | 68 | Er | Erbium |
| 10 | Ne | Neon | 69 | Tm | Thulium |
| 11 | Na | Sodium | 70 | Yb | Ytterbium |
| 12 | Mg | Magnesium | 71 | Lu | Lutetium |
| 13 | Al | Aluminum | 72 | Hf | Hafnium |
| 14 | Si | Silicon | 73 | Ta | Tantalum |
| 15 | P | Phosphorus | 74 | W | Tungsten |
| 16 | S | Sulfur | 75 | Re | Rhenium |
| 17 | Cl | Chlorine | 76 | Os | Osmium |
| 18 | Ar | Argon | 77 | Ir | Iridium |
| 19 | K | Potassium | 78 | Pt | Platinum |
| 20 | Ca | Calcium | 79 | Au | Gold |
| 21 | Sc | Scandium | 80 | Hg | Mercury |
| 22 | Ti | Titanium | 81 | Tl | Thallium |
| 23 | V | Vanadium | 82 | Pb | Lead |
| 24 | Cr | Chromium | 83 | Bi | Bismuth |
| 25 | Mn | Manganese | 84 | Po | Polonium |
| 26 | Fe | Iron | 85 | At | Astatine |
| 27 | Co | Cobalt | 86 | Rn | Radon |
| 28 | Ni | Nickel | 87 | Fr | Francium |
| 29 | Cu | Copper | 88 | Ra | Radium |
| 30 | Zn | Zinc | 89 | Ac | Actinium |
| 31 | Ga | Gallium | 90 | Th | Thorium |
| 32 | Ge | Germanium | 91 | Pa | Protactinium |
| 33 | As | Arsenic | 92 | U | Uranium |
| 34 | Se | Selenium | 93 | Np | Neptunium |
| 35 | Br | Bromine | 94 | Pu | Plutonium |
| 36 | Kr | Krypton | 95 | Am | Americium |
| 37 | Rb | Rubidium | 96 | Cm | Curium |
| 38 | Sr | Strontium | 97 | Bk | Berkelium |
| 39 | Y | Yttrium | 98 | Cf | Californium |
| 40 | Zr | Zirconium | 99 | Es | Einsteinium |
| 41 | Nb | Niobium | 100 | Fm | Femium |
| 42 | Mo | Molybdenum | 101 | Md | Mendelevium |
| 43 | Tc | Technetium | 102 | No | Nobelium |
| 44 | Ru | Ruthenium | 103 | Lr | Lawrencium |
| 45 | Rh | Rhodium | 104 | Rf | Rutherfordium |
| 46 | Pd | Palladium | 105 | Db | Dubnium |
| 47 | Ag | Silver | 106 | Sg | Seaborgium |
| 48 | Cd | Cadmium | 107 | Bh | Bohrium |
| 49 | In | Indium | 108 | Hs | Hassium |
| 50 | Sn | Tin | 109 | Mt | Meitnerium |
| 51 | Sb | Antimony | 110 | Ds | Darmstadtium |
| 52 | Te | Tellurium | 111 | Rg | Roentgenium |
| 53 | I | Iodine | 112 | Cn | Copernicium |
| 54 | Xe | Xenon | 113 | Uut | Ununtrium |
| 55 | Cs | Cesium | 114 | Uuq | Ununquadium |
| 56 | Ba | Barium | 115 | Uup | Ununpentium |
| 57 | La | Lanthanum | 116 | Uuh | Ununhexium |
| 58 | Ce | Cerium | 117 | Uus | Ununseptium |
| 59 | Pr | Praseodymium | 118 | uuo | Ununoctium |
Saat melihat tabel yang asli, cara membaca sistem periodik yang benar adalah dari bagian kiri atas ke arah kanan bawah. Setiap unsur sudah disusun berdasarkan nomor atomnya, yang paling kecil ada di kiri atas dan yang paling besar ada di kanan bawah.
Nomor atom sendiri menunjukkan jumlah proton yang dimiliki oleh atom di setiap unsur kimia. Semakin besar nomor atomnya artinya massa atom juga semakin besar. Pertambahan massa atom dihitung dengan jumlah neutron dan proton yang ada di atom unsur kimia.
Baca juga: Proses Penagihan Amar Bank dan Cara Atasi Gagal Bayar
Untuk bisa memahami tabel periodik dan membaca tabel dengan benar, pelajari dulu pengertian tabel unsur kimia dan apa saja yang mendasari penggolongan atau pengelompokan unsur kimia tersebut. Kemudian coba membaca tabel unsur kimia dengan cara yang benar.